On réalise la combustion complète d’un volume V=10 cm3 d’un alcyne A. le volume de dioxyde de carbone formé est V1=50 cm3. les volumes sont mesurés dans les conditions normales de températures et de pression.
1.1. Écrire l’équation bilan de la réaction.
1.2. Déterminer la formule brute de A ainsi que le volume de dioxygène utilisé.
1.3. Écrire toutes les formules semi-développées de l’alcyne A et les nommer.
1.4. L’hydrogénation catalytique sur nickel ou platine de l’un de ces isomères conduit au pentane. Peut-on en déduire quel est cet alcyne?
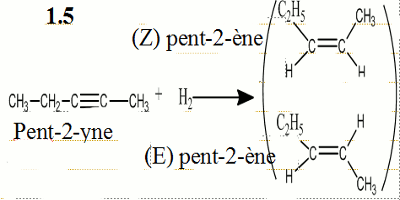
1.5. Par hydrogénation catalytique sur palladium désactivé, A donne B présentant des stéréo-isomères. Déterminer les formules semi-développées de A , B et des stéréo-isomères de B et les nommer.
L’hydratation de B donne deux composés C1 et C2 en quantité égale.
2.1 Donner les conditions expérimentales pour réaliser cette réaction.
2.2 Quelles sont les formules semi-développées et les noms de C1 et C2.
2.3 En utilisant les formules brutes, écrire l’équation bilan de la réaction.
2.4 La masse de B utilisée est mB = 140 g,
Calculer alors la masse du produit obtenue sachant que le rendement de la réaction est de 8%.
2.5 En déduire alors la masse de C1 et C2 dans le mélange.
1.1 Écrivons l’équation bilan de réaction :
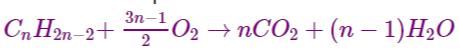
1.2 Formule brute de A
De l’équation bilan, nous avons:
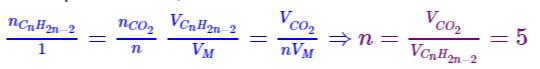
1.3 Formules semi-développées du pentène
Pent-1-yne : CH3−CH2−CH2≡CH
3-méthylbut-1-yne : CH−CH(CH3)−C≡CH
Pent-2-yne : CH3−CH2−C≡C−CH3
1.4 C’est alcyne est le pent-1-yne
2.1 il suffit d'utiliser un acide dilué. L'ion H+ est alors un catalyseur de la réaction :
2.2 pentan-2-ol et pentan-3-ol
2.3 Équation de réaction C5H10+H2OC5H10+H2O →C5H12O→C5H12O
2.4 Calcule de la masse du produit : A chercher