I. Une amine aliphatique à chaine saturé A, contient 19,2 %
d’azote.
a) Quelle est sa formule brute ?
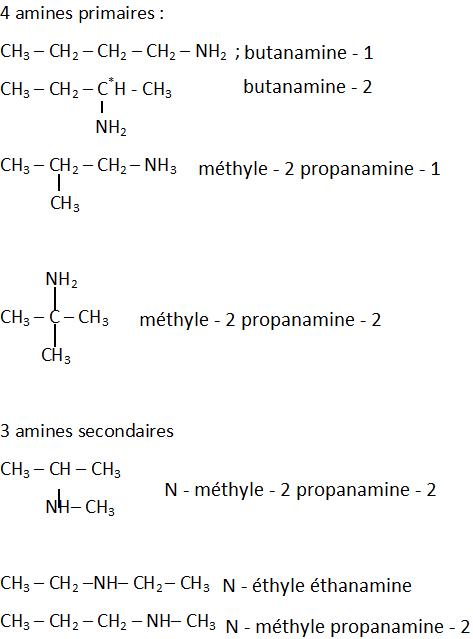
b) Ecrire la formule semi développée et le nom de chacune
des amines correspondantes à cette formule brute
c) Sachant que A est chirale, représenter ses stérèo-isomères
d) Une solution de A de concentration 8.10-2 mol/l a
pH = 11,6. En déduire la constante d’acidité du couple
acide / base
II. On mélange 20 cm3 d’une solution de permanganate de
potassium à 5.10-3 mol/l et 30 cm3 d’une solution d’acide
éthanoïque à 5.10-2 mol/l .
a) Ecrire l’équation de la réaction
b) Calculer la quantité de matière d’ion permanganate
initialement présent dans le mélange
c) En déduire la quantité de matière d’acide éthanoïque qui
n’a pas pu etre oxydé au cours de la réaction
I. Chimie Organique
a) Formule brute de l’amine A
La formule générale des amines allphatique
saturées est : CnH2n + 1 – NH2 ou CnH2n + 3 – N
On a : %N = (14/M) ⇒ M= (14/N) × 100 = 73g/mol
D’autre part M = 14n + 17⇒ n = (M- 17)/ 14 = 4
D’où la formule brute de A C4H11N
b) Formules semi-développées et noms des amines
isomères

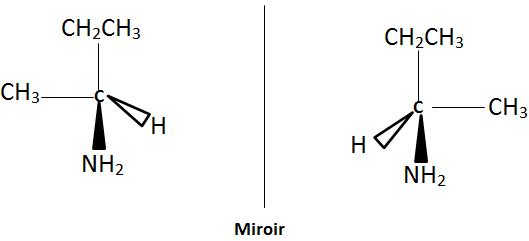
Les stéréo-isomères de A
La butanamine – 2 contient un carbone asymétrie, elle est donc chirale. Elle admet deux stéréo-isomères image l’un et l’autre dans un miroir
d) Calculons la constante d’acidité du couple
En appliquent les lois générales relatives aux solutions aqueuse, on trouve
Ka = 1,9 10.-11
II. Cinétique chimiques
Schéma d’expérience
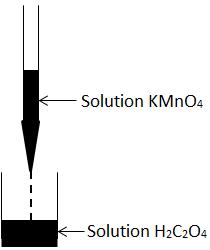
a) Equation bilan de la réaction
Couple redox : KMnO4/Mn2+ et CO2 / H2C2O4
Demi équations rédox
2/ MnO4 + 8H+ + 5e- → Mn2+ + 4H2O
5/ H2C2O4 - 2e- → 2CO2 + 2H+
2 MnO4 - + 5 H2C2O4 + 6 H+ → 2 Mn2+ + 10CO2 + 8H2O
2 MnO4 - + 5 H2C2O4 + 6H3O+ → 2 Mn2+ + 10CO2 + 14H2O
b) Calculons la quantité initiale d’ion permanganate MnO4-
n MnO4- = n1 = nox = 0,001mol/l
c) Quantité d’acide éthanoïque non oxydé
On a : nres H2C2O4 = n0 H2C2O4 - ndisp H2C2O4
Déterminons:
n0 H2C2O4 = nred = Cred Vred ⇒
n0 H2C2O4= 5.10-2 × 3.10-2 = 15.10-4mol
D’autre part, d’après l’équation de la réaction
n MnO4-/2 =ndisp H2C2O4/5 ⇒ ndisp H2C2O4 = (5/2) n MnO4- = 2,5.10-4 mol
Ainsi nres H2C2O4 = n0 H2C2O4 - ndisp H2C2O4 = 1,25.10-3mol
nres H2C2O4 = n2 = 1,25.10-3mol = 0,00125mol