Théorie
1) Comment peut on reconnaître qu’une substance est dextrogyre ou lévogyre. Réprésenter dans l’espace les deux énantiomères de l’acide amino – 2 propénoique.
2) La densité de vapeur d’un alcool secondaire saturé est d = 2,52. Déterminer la formule et le nom de cet alcool .
Pratique
Quel volume d’hydroxyde de sodium de concentration
10-2 mol/l faut il ajouter à un volume de 30 cm3 d’un solution d’acide éthanoique de concentration 10-2 mol/l pour avoir une solution de pH = 5,05 ?
Le pKA du couple CH3COOH/CH3COO- est 4,75
Théorie
1) On reconnaît qu’une substance est dextrogyre ou lévogyre par son action sur la lumière polarisée .
Quand la rotation a lieu dans le sens de l’aiguille d’une montre, la substance est dite dextrogyre.
Quand la rotation a lieu dans le sens inverse, la substance est dite lévogyre.
Représentation spatiale de l’acide amino – 2 propénoique
l’acide amino – 2 propénoique a pour formule
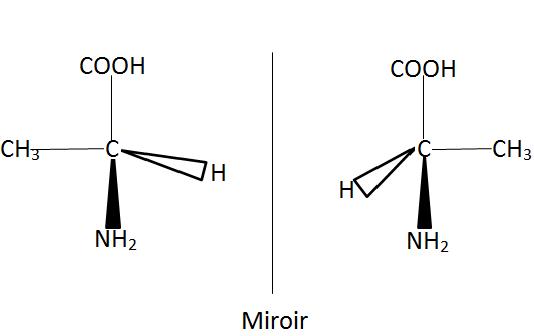
2) Déterminons la formule et le nom de l’alcool secondaire
Soit CnH2n+1OH, la formule brute de cet alcool
Sa masse molaire approchée est :
M = 29d = 73,08g/mol ≈ 73 g/mol
D’autre part : M = 14n +18 = 73 ⇒ n = 4
D’où C4H10O
L’alcool secondaire correspondant à cette formule brute est le butanol – 2 de formule semi développée
CH3 – CH2 – CHOH – CH3
Remarque le butanol – 2 possède un carbone asymétrie
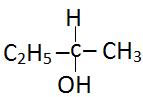
Les deux énantiomères sont représentés ci-dessous
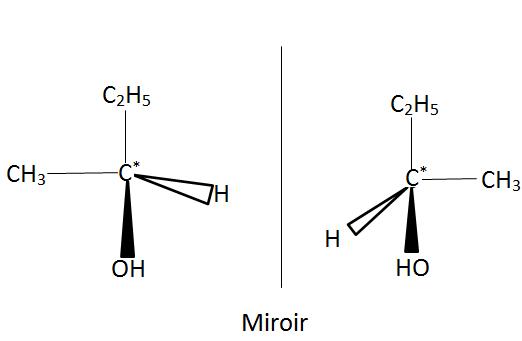
Pratique
1) Calculons le volume d’hydroxyde de sodium l’équation bilan de la réaction s’écrit :
CH3COOH + OH- → CH3COO- + H3O+
Bilan des espèces chimiques : H3O+ ; OH- ; Na+ ; CH3COO- ;CH3COOH
D’après la relation d’Anderson
pH = pKA + log [CH3COO-]/[CH3COOH] ⇒
log [CH3COO- ]/[CH3COOH] = pH – pKA ⇒
[CH3COO-]/[CH3COOH] = 10pH-pKA = 10-3 = 2
soit : [CH3COO-] = 2[CH3COOH] (1)
déterminons [CH3COO-] et [CH3COOH]
L’électroneutrlité de la solution impose
[H3O+] + [Na+] = [OH-] + [CH3COO-] ⇒
[CH3COO-] = [Na+] = CbVb/ (Va +Vb)
La conservation de la matière donne
[CH3COO-]+ [CH3COOH] = CaVa/ (Va + Vb)⇒
[CH3COOH] = (CaVa - CbVb)/(Va + Vb)
la solution impose
[H3O+] + [Na+] = [OH-] + [CH3COO-]⇒
[CH3COO-] = [Na+] = CbVb/ (Va +Vb)
La conservation de la matière donne
[CH3COO-] + [CH3COOH] = CaVa/ (Va + Vb)⇒
[CH3COOH] = (CaVa - CbVb)/(Va + Vb)
En remplaçant ces concentrations dans (1) on obtient : Vb = 2(Va - Vb) ⇒ 3Vb = 2Va⇒
Vb = 2/3 (Va) = 60/3 = 20 cm3
Vb = 20 cm3