I.
A) Quels volumes de solution d’ammoniac de concentration 0,02 mol/l et de chlorure d’ammonium de meme concentration faut – il mélanger pour avoir 100 ml de solution de pH = 9,4 ? Le pKA = du couple NH4+ / NH3 est 9,2 ?
B) calculer les concentrations des espèces chimiques en solution.
Données : 10-9,2 = 4. 10-10 ; 100,15 = 1,41.
II.
Un acide carboxylique A réagi avec un alcool B pour un produit C de masse molaire
M = 88 g/mol et de l’eau.
a) Ecrire l’équation de la réaction à l’aide des formules générales des acides carboxyliques et les alcools
b) Sachant que la masse molaire de B est M = 46 g/mol et que l’oxydation de B par le bichromate de potassium en milieu acide donne un produit qui réagit avec la liqueur de Fehling, déterminer les formules semi développées exacte de B et C.
c) On designe par D l’anhydride l’acide correspondant à A. Expliquer comment on D à partir de A. Ecrire l’équation de la réaction correspondante à l’aide des formules semi développées.
d) Quelles différences y a-t-il entre l’action de A sur B et de
e) Calculer la masse de chacun des produits obtenus par l’action de 15g de D sur 6g de B si le rendement de cette réaction est 70%.
f) Y a-t-il un réactif en excès ? quel est la masse de ce réactif ?
I.
A) Calculons les volumes d’ammoniac et de chlorure d’ammonium
Le mélange est le siège de deux équilibres
NH3 + H2O  NH4+ + OH-
NH4+ + OH-
NH4+ + H2O  NH3 + H3O+
NH3 + H3O+
Bilan des espèces : H3O+ ; OH- ; Cl- ; NH3 ; NH4+.
Le volume du mélange obtenu est
Va + Vb = 100 ml = 0,1 l (1)
Exprimonsles concentrations des diverses espèces chimiques
pH = 9,2 ⇒ [H3O+] = 10-pH = 10-9,2 = 4.10-10 mol/l
[OH- ] = 10-14 /[H3O+] = 2,5.10-5 mol/l;
[Cl-] = CaVa/(Va + Vb) = 0,1Va mol/l;
La neutralité électrique de la solution impose
[NH4+] = [Cl-] + [OH- ] - [H3O+] ≈ [Cl-]= 0,1Va mol/l
[NH3] + [NH4+] = (CaVa + CbVb) /(Va + Vb) ⇒
[NH3] = CbVb /(Va + Vb) = 0,1Vb mol/l
D’autre part d’après la relation d’Anderson
pH = pKA + log [NH3]/[NH4+] ⇒ log [NH3]/[NH4+] = pH – pKA
soit log Vb/Va = 9,4 – 9,25 = 0,15 ⇒ Vb/Va = 100,15 = 1,41.
D’où Vb = 1,41Va (2) D’où
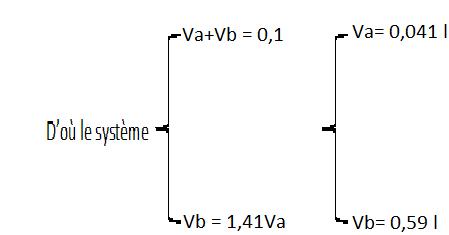
Va = 41 ml ; Vb = 59 ml
b) Calculons la concentrations des espèces chimiques présentent en solution
pH = 9,2 ⇒ [H3O+] = 10-pH = 10-9,2 = 4.10-10 mol/l
(Cl-) = CaVa/(Va + Vb) = 0,1Va mol/l;
or Va = 0,041l ⇒ (Cl-) = 0,041 * 0,1 = 0,0041 mol/l
La neutralité électrique de la solution impose
[NH4+] = [Cl-] + [OH- ] - [H3O+] ≈ [Cl-]= 0,1Va mol/l
[NH3] + [NH4+] = (CaVa + CbVb) /(Va + Vb) ⇒
[NH3] = CbVb /(Va + Vb) = 0,1Vb mol/l
nous savons que : Vb = 0,059 l ⇒ [NH3] = 0,1 * 0,059 = 0,0059 mol/l
II.
a) Equation générale de la réaction de A sur B
CnH2n + 1 – COOH + CmH2m + 1 – OH = ; CnH2n + 1 – COO+ CmH2m + 1 + H2O
b) Déterminons les formules semi développées exactes de C et D
La masse molaire de B est
MB = 14m + 18 ⇒ m = (MB – 18)/14= 2 ⇒ m = 2
La masse molaire de C est
MC = 14(n + m) + 46 ⇒ n + m = 3 ⇒ n = 3 – 2 = 1
D’où la formule semi développée de C et de B
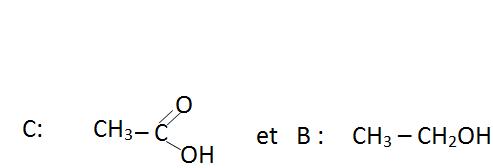
c) Obtention de l’anhydride B à partir de l’acide A.
On obtient l’anhydride à partir de A par déshydratation entre molécules d’acides carboxyliques en présence de P4O10 (déshydratant)
L’équation bilan de la réaction s’écrit
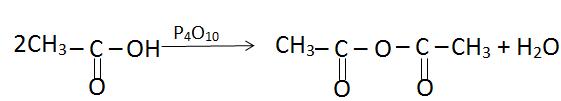 d) Différence entre l’action de A sur B et celle de B sur D
d) Différence entre l’action de A sur B et celle de B sur D
L’estérification de A par B est une réaction lente, limitée et athermique.
L’estérification de D sur B est une réaction rapide, totale et exothermique
e) Calculons la masse de chacun des produits obtenus par action de D sur B
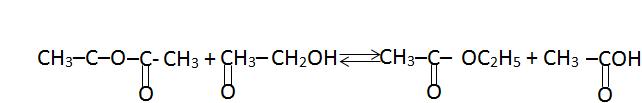 On a : nb = mb/Mb = 6/46 0,13 mol
On a : nb = mb/Mb = 6/46 0,13 mol
nd = md/Md = 15/102 = 0,147 mol
comme nd > na, le compose D est en excès
la masse de chacun des produits obtenus est donc :
masse de l’acide C :
mc = (Mc × r×mb) /Mb = 88 × 70 × 6 /100 × 46 = 8,03 g ⇒
mc ≈ 8g
masse de l’acide A
ma = (Mc × r×mb) /Mb = 60 × 70 × 6 /100 × 46 = 5,47 g ⇒
ma ≈ 5 ,5g
f) Calcul de l’excès de D
La de D ayant réagit est :
md2 = (Md× r × mb) /Mb = 102×70 × 6 /100 × 46 = 9,3 g
l’excès D est alors : m = md1 – md2 = 15 – 9,3 = 5,7g
d’où m = 5,7 g
m = 5,7 g