A la date t = 0, on laisse tomber 1g de magnésium dans
30 cm3 d’une solution de chlorure d’hydrogène de concentration 0,1 mol/l. Le tableau ci-dessous présente l’évolution de la concentration des ions H3O+ au cours du temps
| t(min) | 0 | 1 | 2 | 3 | 4 | 5 |
| [H3O+ ].10-1 | 1,0 | 0,50 | 0,355 | 0,25 | 0,16 | 0,10 |
1) Ecrire l’équation bilan de la réaction
2) Déterminer l’expression de la concentration des ions magnésium à la date t en fonction de la concentration des ions H3O+ à cet instant. Calculer la valeur de la concentration des ions de magnésium aux dates
t1 = 2 min ; t2 = 4 min.
3) Définir la vitesse moyenne de formation des ions magnésium entre 2 et 4 min, puis calculer sa valeur
I.
A 10cm3 de solution d’acide chlorhydrique de concentration 2.10-2 mol/l , on ajoute 10 cm3 d’une solution d’hydroxyde de sodium de concentration 10-2 mol/l.
1) Ecrire l’équation bilan de la réaction
2) Peut-on atteindre l’équivalence acido-basique ? Préciser si la solution obtenue est acide, basique ou neutre
3) Déterminer le pH de la solution
4) Calculer les concentrations espèces chimiques présentes dans la solution ; On donne log5 = 0,7
II.
Une oxydation ménagée à l’aide du permanganate de potassium en milieu acide d’un produit A conduit à un produit B dont la solution aqueuse a un pH < 7 à 25°C. B permet obtenir un chlorure acyle C de formule
CH3 – CH2 – COCl par un procédé à préciser.
C réagit avec l’ammoniac pour donner du chlorure d’hydrogène et un produit D.
C réagit avec A pour donner du chlorure d’hydrogène et un produit E.
1) Ecrire les équations des réactions successives.
2) Ecrire la formule semi développée et le nom de chacun des composés A ;B ;D ; et E
1) Equation bilan de la réaction
1/2/Mg → Mg2+ + 2e-
1/2/2H+ + 2e- → H2
Mg + 2H+ → Mg2+ + H2
Ou Mg + 2 H3O+ → Mg 2+ + H2 + 2 H2O
L’équation molaire s’écrit
Mg + 2HCl → MgCl + H2
2) Calculons la concentration des ions magnésium en fonction de [H3O+]
D’après l’équation de la la réaction : [Mg2+] = 1/2[H3O+]disp
Or [H3O+]disp = [H3O+]0 - [H3O+]rest == [H3O+]disp = Ca - [H3O+]rest
D’ou [Mg2+] = ½(Ca - [H3O+]rest) mol/l
Calculons la valeur de la concentration des ions magnésium aux dates t1 = 2 min, et t2 = 4 min
A la date t1 = 2 min ; [H3O+] rest = 0,355 mol/l
Mg2+] = ½(0,1 - 0,355) = 0 ,03225mol/l = 3,225.10-2mol/l
A la date t2 = 4 min ; [H3O+] rest = 0,16 mol/l
Mg2+] = ½(0,1 - 0,16) = 0,042= 4,2.10-2mol/l
3) Vitesse moyenne de formation des ions magnésium
Par définition : Vm = Δ[Mg2+]/Δt = ΔC/ Δt
La vitesse moyenne de formation des ions magnésium entre
t1 = 2 min et t2 = 4 min est :
Vmf = Δ[Mg2+]/Δt = (8,4.10-2 – 6,45.10-2)/(4 -2) =
0,975.10-2mol/l.min == Vmf = 9,75.10-3mol/l.min
NB : la donnée de la masse est inutile (piège)
ACIDE ET BASES SOLUTION AQUEUSE
1) Equation bilan de la réaction
(H3O+ + Cl-) + (Na+ + OH-) → (Na+ + Cl-) + H2O
H3O+ +OH- →2 H2O
2) Nature de la solution obtenue
Les quantités initiales de l’acide et de la base mises en solution sont :
na = CaVa = 2.10-2. 10-2 = 2.10-2mol/l
nb = CbVb = 10-2 10-2 = 10-4mol/l
na > nb ; l’acide est en excès, en effet on ne peut atteindre l’équivalence et la solution obtenue est acide
3) Déterminons le pH de la solution
nH3O+ = na – nb ; or [H3O+] = nH3O+/vf = (na – nb)/ vf ;
alors que pH = -log[H3O+] ⇒pH = -log(na – nb)/ vf = 2,3
pH = 2,3
4) Calculons les concentrations des différentes espèces chimiques présentes dans la solution
Bilan des espèces chimiques : H3O+ ; OH- ; Cl- ; Na+
[H3O+] = 10-pH = 10-2,3 = 5. 10-3 mol/l
[OH-]= 10-14/ [H3O+] = 2. 10-12 mol/l
[Cl-] = (CaVa)/(Va + Vb) = 10-2 mol/l
[Na+]= CbVb/ (Va + Vb) = 5.10-3 mol/l
II. CHIMIE ORGANIQUE
1) Equations des réactions successives
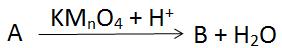
Le chlorure d’acyle C, résulte de l’action sur un argent chlorurant ; le chlore de thionyle SOCl2, par exemple
B + SOCl2 → CH3 – CH2 – COCl + SO2 + HCl
CH3 – CH2 – COCl + NH3 → HCl + D
CH3 – CH2 – COCl + A → HCl + E.
2) Les formules semi développée et les noms des composés A , B , D , E
A : est alcool primaire : CH3 – CH2 – CH2OH
B :est acide carboxylique : CH3 – CH2 – COOH