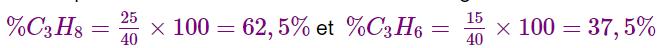La combustion complète de 40 mL d'un mélange de propane et de propène a nécessité 192,5 mL de dioxygène.
Quelle est la composition centésimale en volume du mélange ?
Soit V1 le volume de propane et V2 le volume de propène : V1+V2=40 mL
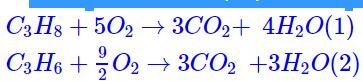
Les équations de combustion des constituants du mélange sont les suivantes:
De la relation (1), nous avons :
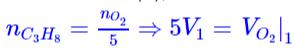
De la relation (2) nous avons :
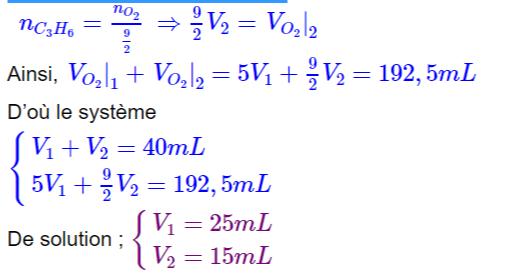
La composition centésimale en volume du mélange est dont :