On réalise en présence d’un catalyseur peu actif l’hydrogénation du but-1-yne et on obtient un composé (A).
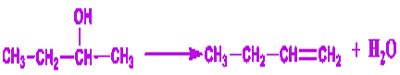
1. Ecrire l’équation d’hydrogénation du but-1-yne et préciser le nom et formule semi développée de A.
2. Par hydratation de A on obtient un mélange de deux composés B et C.
Ecrire l’équation de l’hydratation de A et donner les formules semi développées et les noms de B et C.
3. B est le produit majoritaire. on verse une masse de B sur 40g de sodium. on recueille 3,36L d’un gaz qui fait une détonation en présence d’une flamme.
3.1. Ecrire l’équation de la réaction
3.2. Déterminer la masse m de B versée et la masse de sodium restante. On donne volume molaire V0 = 22.4 mol/L.
4. La déshydratation intermoléculaire de B donne un composé D.
Ecrire l’équation de déshydratation et préciser le nom de B.
1. Équation de réaction
CH2−CH2−C≡CH+H2→ CH3−CH2−CH=CH2
Le produit obtenue est le but-1-ène
2. Équation de hydratation de A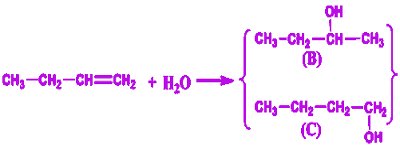
(B) Butan-2-ol (C) Butan-1-ol.
3.1 Équation de réaction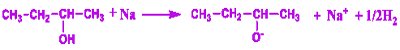
Le gaz qui détone en présence de la flamme est le dihydrogène.
3.2 Calcule de la masse de B
De l’équation de réaction, on a
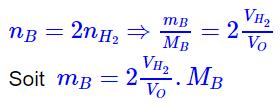
AN :mB = 22,2g
La masse de Na ayant réagit est d’après l’équation de réaction nNa=2nH2⇒
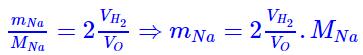
La masse de sodium restante est donc;
mNa)restante = mNa)initiale − mNa)reagitm =40−6,9=33,1g=33,1g
4 Écrivons l’équation de déshydratation intramoléculaire de B